Protezy biodra wszczepiane pacjentom od 2003 roku na całym świecie mają być potencjalnie toksyczne. Amerykański producent, firma DePuyOrthopaedics, wiedziała o tym, ale zrobiła wszystko, żeby to ukryć. Ma to dotyczyć kilkadziesięciu tysięcy pacjentów w Europie, aczkolwiek we Francji protezy te zastosowano u jedynie 380 osób. Francuska agencja zdrowotna AFSSAPS zareagowała na tę sytuację, co oczywiste, ale na dzień dzisiejszy nie zmienia swoich zaleceń.
Bezpieczeństwo urządzeń medycznych ponownie zasiada na gorącym krześle, tuż po tym, jak jego wiarygodność została podburzona przez skandal z protezami piersiowymi PIP.
Zaczęło się od informacji, które zostały podane do wiadomości publicznej w Wielkiej Brytanii i Francji, odnośnie wadliwych protez biodrowych. Setki tysięcy pacjentów na całym świecie może mieć aktualnie kontakt z bardzo wysokimi poziomami metalami toksycznymi, z powodu pewnego modelu protezy biodra, o czym zaalarmowały brytyjski magazyn medyczny British Medical Journal (BMJ) i BBC we wspólnym komunikacie, który pokazywał, że ryzyko było bardzo dobrze znane producentowi amerykańskiemu.
Francuski magazyn Le Figaro również potwierdził, że firma DePuyOrthopaedics, filia Johnson & Johnson, zrobiła wszystko, aby utrzymać te protezy na rynku, mimo niepokojących sygnałów. Aż do lata 2010 roku, firma sprzedawała je w Europie, a przede wszystkim we Francji, mimo pierwszych alarmowych sygnałów, które pojawiły się w Australii już w 2007 roku, jak podaje magazyn Le Figaro.
Możliwość wszczepiania protez biodra to jeden z największych sukcesów współczesnej medycyny, mówi pani Fiona Godlee, redaktor naczelna BMJ. Ale połącznie niewłaściwej regulacji oraz merkantylizmu bez granic spowodowało prawdziwe zło, zagrażające potencjalnie wielkiej liczbie pacjentów na całym świecie.
Protezy biodra, tak samo jak implanty piersiowe, to materiały medyczne, a więc nie podlegają one tym samym regulacjom co leki, jeżeli chodzi o ich wprowadzanie na rynek i kontrolę.
Zobacz również:
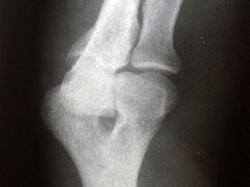
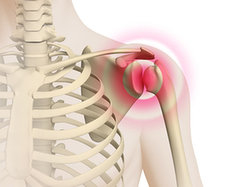
Protezy biodra metal-metal w kolimatorze
Protezy ASR łączą parę „metal-metal”, co jest modelem, który jest uważany za odporny. Ale jego wadą jest to, że może on uwalniać cząsteczki kobaltu i chromu. Stwierdzono dla nich większy poziom konieczności przeprowadzania kolejnych interwencji, w porównaniu do protez innych typów.
Ryzyko wszczepiania implantów na bazie stopu kobaltu i chromu jest znane bardzo dobrze już od 1975 roku, jak uważa brytyjski magazyn medyczny British Medical Journal. Poza reakcjami miejscowymi, które mogą zniszczyć mięśnie i kości, cząsteczki metaliczne mogą również przeniknąć do krwiobiegu.
British Medical Journal oraz BBC cytują dokument wewnętrzny firmy DePuyOrthopaedics z 2005 roku, który przywołuje możliwość, iż pozostałości wynikające ze zużywania protezy mogą być kancerogenne. Oznacza to, że mimo iż ryzyko to było bardzo dobrze znane, z nawet dobrze udokumentowane od dziesięcioleci, pacjentów pozostawiono w błogiej nieświadomości. A tak naprawdę, można powiedzieć, iż brali oni udział, bez swojej wiedzy, w całkowicie niekontrolowanym eksperymencie.
Związek nieustalony, jak uważa AFSSAPS
Protezy ASR pojawiły się na świecie w 2003 roku, do Europy dotarły w 2004 roku. Wszczepiono ich 93 000 pacjentów, w tym 380 we Francji, jak podaje francuska agencja ds. produktów zdrowotnych AFSSAPS.
Każdego roku, we Francji, wszczepia się blisko 100 000 protez biodra, z czego 7% to protezy metal-metal. Między datą wprowadzenia na rynek a marcem 2010 roku, jak francuska agencja AFSSAPS precyzuje, producent tych protez 5 pięć razy złożył raport czujności przed agencją, co oznacza stopę zwrotu 1,3%.
Agencja AFSSAPS powołała więc grupę ekspertów, aby ustalić zalecenia dla wszystkich pacjentów. Rezultat? Na tę chwilę, jak stwierdza francuska agencja ds. produktów zdrowotnych, nie ma możliwości ustalenia formalnego związku między anomalią kliniczną bądź radiologiczną a poszczególnym poziomem jonów metalowych, pochodzących ze składników protezy.
Ten brak anomalii prowadzi agencję AFSSAPS do decyzji o nie zmienianiu zaleceń. Oznacza to, że pacjenci z wszczepionymi protezami biodra będą obserwowani tak, jak zazwyczaj.
Agencja AFSSAPS zaleca jednakże wyjątkową obserwację, roczną albo przedłużoną do 10 lat, dla niektórych pacjentów, przede wszystkim dla tych, u których główka kości udowej ma średnicę większą bądź równą 36 milimetrów. A w końcu, francuska agencja ds. produktów zdrowotnych zdecydowała się zachęcić wszystkich chirurgów do ponownego kontaktu z pacjentami, którym wszczepiono te niesławne protezy, aby poinformować ich o aktualnych zaleceniach.